Le cannabis médical soulage bien les migraines

Pour la première fois, les chercheurs ont mené une étude qui prouve que le cannabis thérapeutique traite les migraines. Une telle étude n’avant jamais été conduite avant à cause des lois fédérales qui empêchent les scientifiques américains d’obtenir du cannabis pour la recherche. Au fil des ans, les personnes souffrant de maux de tête et de migraines se sont tourné vers le cannabis pour soulager leurs douleurs. C’est donc la première fois que des données scientifiques confirment leur revendication.
Les chercheurs de l’Université du Colorado ont rassemblé 121 participants souffrant de migraines. Ils les ont traité avec du cannabis médical entre janvier 2010 et septembre 2014, et ont trouvé que leurs migraines étaient réduites de 10 par mois à moins de 5. La majorité des participants, 103, ont signalé une diminution des migraines. Et seulement 3 personnes ont vu leurs migraines augmenter pendant le test.
Les participants ont utilisé le cannabis de différentes façons, soit en le fumant, soit sous forme « mangeable » (space cake par exemple). L’inhalation s’est montrée la plus efficace pour traiter les migraines, en particulier parce que ses effets arrivent plus rapidement qu’en ingérant le cannabis dans des aliments infusés.
Les chercheurs ont qualifiés les résultats de « considérable » et ont dit qu’ils pouvaient potentiellement déboucher sur de nouveaux traitements contre la migraine dans les 23 Etats où le cannabis thérapeutique est autorisé, ou au moins sur plus de recherches.
Cependant, les chercheurs restent prudents sur la façon dont leurs résultats sont présentés, notant que tout le monde ne doit pas se tourner vers la weed pour guérir leurs maux de tête. Le cannabis affecte toutes les personnes différemment, et peut avoir également des effets négatifs sur la santé.
« Il y a des améliorations conséquentes pour les patients dans leur capacité à fonctionner et à se sentir mieux » dit Laura Borglet, professeure à l’Ecole des Sciences Pharmaceutiques et de Pharmacie de Skaggs et une des auteurs de l’étude. « Comme n’importe quelle drogue, le cannabis a des bienfaits potentiels, tout comme des risques. Il est important pour les gens d’être au courant qu’utiliser du cannabis médical peut aussi avoir des effets négatifs ».
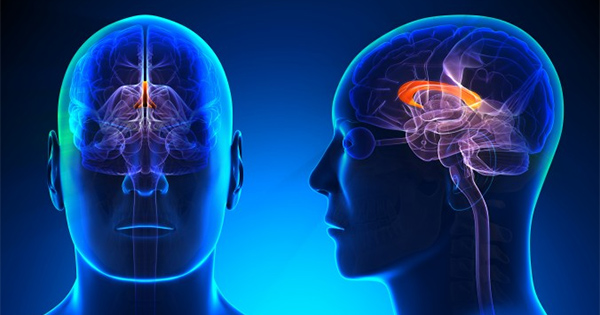
Quoiqu’il en soit, l’étude est un nouvel ajout à un nombre croissant de preuves scientifiques que le cannabis délivre plus de bienfaits pour la santé que la « guerre contre la drogue » aimerait bien l’admettre. Les chercheurs ont encore besoin de déterminer comment le cannabis réduit les migraines. « Nous croyons que la sérotonine joue un rôle dans les maux de têtes, mais nous sommes toujours en train d’ssayer de découvrir le rôle exact des cannabinoïdes » ajoute Laura Borglet.
-
Cannabis au volantil y a 3 semaines
Les consommateurs réguliers de cannabis ne présentent aucune altération de leurs capacités de conduite, selon une nouvelle étude
-
Cannabis en Franceil y a 4 semaines
Cannabis médical : la France légalise enfin !
-
Businessil y a 4 semaines
New York célèbre les cinq ans de la légalisation du cannabis avec 3,3 milliards de dollars de chiffre d’affaires
-
Businessil y a 2 semaines
La DGAL relance sa guerre aux produits CBD
-
Cannabis en Franceil y a 3 semaines
La France prolonge l’accès expérimental au cannabis médical jusqu’en 2027
-
Cannabis en Allemagneil y a 4 semaines
Rapport EKOCAN : la légalisation du cannabis en Allemagne fonctionne… mais pas comme les législateurs l’avaient prévu
-
Cannabis en Franceil y a 4 semaines
7 tonnes de cannabis à Paris : l’ancien patron de l’OCRTIS condamné à un an de prison avec sursis
-
Cannabis en Franceil y a 1 semaine
Amendes cannabis : la Cour des comptes rend un verdict sévère sur la mesure phare de Macron






































Vous devez être connectés pour poster un commentaire Connexion