L’Epidiolex (commercialisé Epidyolex en Europe) est un médicament antiépileptique à base de cannabidiol (CBD) pur, développé par la société britannique GW Pharmaceuticals, aujourd’hui filiale de Jazz Pharmaceuticals. C’est le premier médicament dérivé du cannabis à avoir obtenu l’approbation de la FDA américaine, en juin 2018, et le premier médicament à base de CBD remboursé par l’Assurance maladie en France.
Il se présente sous forme de solution buvable dosée à 100 mg de CBD par millilitre, dissoute dans de l’huile de sésame avec un arôme fraise. Le CBD qu’il contient est extrait de variétés de cannabis légales cultivées
par GW Pharmaceuticals, sélectionnées spécifiquement pour leur haute teneur en cannabidiol et leur très faible teneur en THC.
L’Epidyolex est indiqué chez l’adulte et l’enfant de 2 ans et plus dans trois situations :
Syndrome de Dravet (SD) : épilepsie génétique sévère à début précoce, caractérisée par des crises convulsives fréquentes et prolongées résistant aux traitements antiépileptiques classiques. Le SD touche environ 1 enfant sur 15 000 à 20 000.
Syndrome de Lennox-Gastaut (SLG) : forme grave d’épilepsie de l’enfant associant plusieurs types de crises et une déficience intellectuelle. La pharmacorésistance y est particulièrement marquée.
Sclérose tubéreuse de Bourneville (STB) : maladie génétique rare pouvant provoquer des tumeurs bénignes dans plusieurs organes, dont le cerveau, et entraîner une épilepsie sévère. Dans cette indication, le remboursement est restreint aux patients présentant une épilepsie pharmacorésistante.
Dans tous les cas, l’Epidyolex est prescrit en association avec d’autres antiépileptiques, notamment le clobazam pour le SD et le SLG.
Les essais cliniques de phase 3 ont démontré que chez les patients atteints du syndrome de Dravet ou de Lennox-Gastaut, l’Epidyolex réduit significativement la fréquence des crises par rapport au placebo. Les données FDA-approuvées montrent que 47% des patients traités constatent une réduction d’au moins 50% de leurs crises après 12 semaines de traitement — un résultat considérable pour des pathologies où les options thérapeutiques sont extrêmement limitées.
La HAS (Haute Autorité de Santé) a reconnu l’Epidyolex comme représentant « un progrès thérapeutique » dans le traitement de ces deux syndromes chez les patients de 2 ans et plus.
ATU nominative (2017-2019) : disponible en France dès 2017 via autorisation temporaire d’utilisation nominative, uniquement dans les pharmacies hospitalières.
AMM européenne (2019) : le 19 septembre 2019, la Commission européenne accorde une autorisation de mise sur le marché valable dans toute l’Union européenne, sous le nom Epidyolex.
Autorisation d’accès compassionnel (2019-2022) : en attente de la fixation du prix et du remboursement, Epidyolex est accessible via le dispositif d’accès compassionnel.
Remboursement (décembre 2022) : Epidyolex obtient son prix et son remboursement en France par arrêté du 14 décembre 2022 — une première historique pour un médicament à base de cannabis. Le médicament est depuis disponible en pharmacie de ville et remboursé à 65% par l’Assurance maladie.
Prix : 1 066,74 euros le flacon de 100 mL (remboursé à 65%, soit environ 373 euros restant à charge avant mutuelle).
Prescription : initiale hospitalière annuelle, réservée aux spécialistes en neurologie et neuropédiatrie. Renouvellement possible par tout médecin.
L’Epidiolex est approuvé et commercialisé dans plus de 30 pays, dont les États-Unis (FDA, juin 2018), l’ensemble des pays de l’Union européenne (EMA, 2019), le Royaume-Uni, le Canada et l’Australie. Aux États-Unis,
il est également approuvé pour la sclérose tubéreuse de Bourneville chez les patients d’un an et plus.
→ Voir aussi : GW Pharmaceuticals, l’entreprise britannique qui a développé l’Epidiolex et le Sativex


Pharma 5, l’un des principaux laboratoires pharmaceutiques du Maroc, vient d’annoncer la mise sur le marché prochaine du premier médicament thérapeutique à base de cannabis du...


Les consommateurs de Newsweed les plus réguliers l’auront remarqué, nous étions en pause ces dernières semaines. Mais puisque l’actualité ne nous attend pas, voici un récapitulatif...


Le Laboratoire national des médicaments du Portugal (LNM), une institution relevant du ministère portugais de la défense, avance sur la production de cannabis médical selon les...
Dans un communiqué de presse, Jazz Pharmaceuticals Canada a annoncé que Santé Canada a approuvé l’utilisation de l’Epidiolex®, une huile CBD pharmaceutique, comme traitement de certaines formes...


Avec un secteur du CBD européen en pleine expansion, malgré un bourbier réglementaire, des centaines d’acteurs industriels de part et d’autre de l’Atlantique sont confrontés à...


Le fabricant d’Epidiolex, un médicament à base de CBD délivré sur ordonnance, a intenté une action en justice aux États-Unis pour violation de brevet. GW Research,...
Disponible en France depuis 2018 par le biais d’autorisations temporaires d’utilisation (ATU) nominatives avant de décrocher son autorisation de mise sur le marché (AMM) européenne le...


Le ministère japonais de la Santé, du Travail et des Affaires sociales a déclaré fin septembre qu’il soutenait un amendement à la loi sur les drogues...


Quatre mois après avoir pris connaissance du rapport du Comité technique sur le cannabis à usage médical, le gouvernement mauricien a donné son accord pour le...


Jazz Pharmaceuticals, société pharmaceutique irlandaise, a annoncé avoir conclu un accord pour acheter 7,2 milliards $ (6 milliards €) en espèces et en actions le fabricant...


Alors qu’il a fallu 2 ans et demi à Billy Caldwell pour obtenir son traitement à base de cannabis pour traiter son épilepsie, l’association britannique End...


L’Epidyolex, l’huile CBD médicale de GW Pharmaceuticals, a reçu l’approbation de la Therapeutic Goods Administration (TGA), l’organe de régulation des médicaments en Australie, pour être utilisée...


GW Pharmaceuticals a annoncé lundi que l’Epidiolex, un médicament à base de cannabidiol (CBD) utilisé dans le traitement de l’épilepsie, avait été retiré de l’annexe V...


La prescription et le remboursement de deux médicaments à base de cannabis ont été approuvés par le système de santé publique anglais (NHS). L’organisme de surveillance...


La Commission Européenne a approuvé l’autorisation de mise sur le marché (AMM) de l’Epidyolex, le nom européen de l’Epidiolex, comme traitement d’appoint des crises associées au...
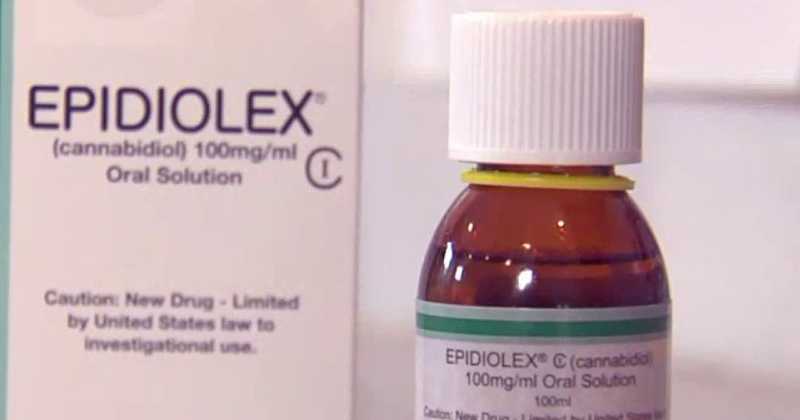

Un panel de l’Agence Européenne des Medicaments (EMA) a rendu vendredi un avis favorable pour l’Epidiolex, une huile de CBD qui sert à traiter les cas...


La Corée du Sud, pourtant conservatrice sur la question du cannabis, vient de devenir le premier pays d’Asie de l’Est à légaliser le cannabis médical. Cette...


La décision de la DEA la semaine dernière de placer l’Epidiolex, un médicament à base d’huile de cannabidiol (CBD), hors de l’annexe 1 des substances contrôlées...
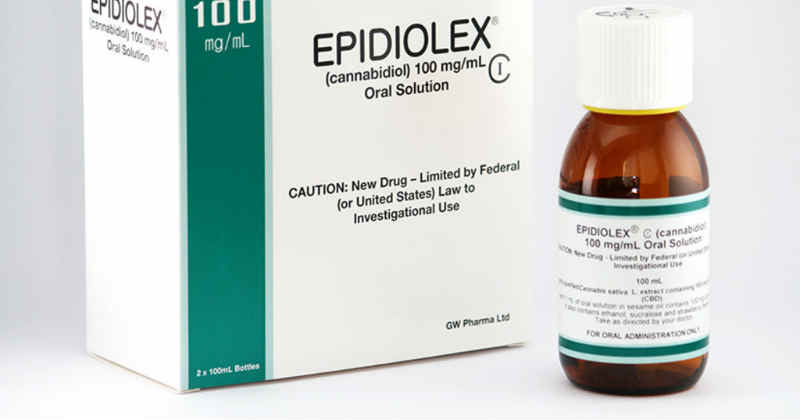

En Juin, la Food and Drug Administration américaine approuvait le médicament Epidiolex, une huile de CBD visant à traiter certains cas d’épilepsie. A la suite de...


Alors que les recherches sur les possibilités du cannabis et ses vertus thérapeutiques commencent à se multiplier, tous les pays ne mettent pas à disposition les...
Vous devez être connecté pour poster un commentaire.