Le Sativex (dénomination commune internationale : nabiximols) est un médicament à base d’extraits de cannabis développé par GW Pharmaceuticals, aujourd’hui filiale de Jazz Pharmaceuticals. C’est le premier médicament dérivé du cannabis à avoir obtenu une autorisation de mise sur le marché dans le monde — au Royaume-Uni en 2010 — et le médicament cannabis le plus largement approuvé à l’international avec une présence dans plus de 30 pays.
Il se présente sous forme de spray buccal. Sa composition est unique : il contient des quantités approximativement égales de THC et de CBD — un ratio 1:1 — extraits de deux variétés de cannabis différentes cultivées par GW Pharmaceuticals. Ce ratio, loin d’être arbitraire, s’inspire de la composition des médicaments à base de cannabis utilisés aux XIXe et XXe siècles, comme l’avait établi le fondateur de GW, Geoffrey Guy, en étudiant la littérature médicale historique.
Le Sativex est indiqué dans le traitement symptomatique de la spasticité modérée à sévère due à la sclérose en plaques (SEP), chez les patients adultes qui n’ont pas répondu de manière adéquate aux autres traitements antispastiques.
La spasticité (contractions musculaires involontaires, rigidité, douleurs) touche jusqu’à 80% des patients atteints de SEP à un stade avancé. Elle constitue l’un des symptômes les plus invalidants de la maladie, affectant la marche, le sommeil, l’habillage et tous les gestes quotidiens. En France, environ 5 000 patients pourraient potentiellement bénéficier du Sativex.
Les données cliniques sur le Sativex montrent une efficacité réelle mais limitée à une sous-population de patients. Les études identifient environ 10% de patients « répondeurs » — ceux chez qui le Sativex apporte une réduction significative de la spasticité après 4 semaines d’essai thérapeutique. Pour ces patients, l’amélioration peut être substantielle et durable. Pour les autres, le bénéfice est insuffisant pour justifier la poursuite du traitement.
C’est précisément cette efficacité limitée à une minorité de patients qui a conduit la HAS à juger le Service Médical Rendu « faible » et l’amélioration du SMR « inexistante », deux conclusions qui ont pesé lourd dans le blocage français.
L’histoire du Sativex en France est un cas d’école des blocages bureaucratiques et économiques qui freinent l’accès aux médicaments cannabis médical dans le pays.
2014 : AMM accordée, mais… Le 8 janvier 2014, l’ANSM accorde au Sativex son autorisation de mise sur le marché en France pour la spasticité liée à la SEP. La HAS rend un avis favorable au remboursement à 15% en octobre 2014. Tout semble en ordre.
2015 : le blocage tarifaire La commercialisation est bloquée avant même le lancement : le laboratoire Almirall, distributeur français, demande un prix d’environ 350 euros par mois (20% en dessous du prix européen moyen de 440 euros). Le CEPS propose environ 60 à 70 euros par mois. L’écart est insurmontable.
2016-2021 : les négociations s’enlisent Malgré les interpellations répétées de patients, d’associations et de parlementaires, aucun accord n’est trouvé. Des patients en grève de la faim attirent l’attention des médias. Le médicament reste commercialisé dans 17 puis 23 pays européens, tandis que les patients français doivent se le procurer à l’étranger à leurs frais.
2022 : nouvelle tentative En juillet 2022, Almirall soumet une nouvelle demande d’évaluation à la HAS, appuyée sur de nouvelles données cliniques. La commission de transparence maintient ses conclusions : SMR faible, absence d’amélioration du SMR. Les discussions tarifaires reprennent, sans aboutir.
Aujourd’hui Le Sativex dispose toujours de son AMM en France, mais n’est toujours pas commercialisé ni remboursé. Aucune officine française ne le délivre. Les patients qui souhaitent y accéder doivent se rendre à l’étranger ou tenter d’obtenir une autorisation d’importation — un parcours complexe que seuls les patients les plus informés et les plus aisés parviennent à accomplir.
Le Sativex est approuvé et commercialisé dans plus de 30 pays, dont le Royaume-Uni (premier pays, 2010), l’Espagne, l’Allemagne, l’Italie, le Danemark, la Suède, la République tchèque, le Canada, l’Australie et de nombreux États américains. En Allemagne, il est remboursé par les caisses d’assurance maladie. Au Royaume-Uni, il est disponible sur prescription mais non recommandé par le NICE en raison d’un rapport coût-efficacité
jugé défavorable.
La France et la Slovénie sont les deux seuls pays de l’Union européenne à avoir accordé une AMM au Sativex sans le commercialiser.
→ Voir aussi : GW Pharmaceuticals, l’entreprise britannique qui a développé le Sativex et l’Epidiolex


Le Laboratoire national des médicaments du Portugal (LNM), une institution relevant du ministère portugais de la défense, avance sur la production de cannabis médical selon les...


Un important essai clinique examinant le rôle du Sativex, un médicament à base de cannabis, dans le traitement des tumeurs cérébrales les plus agressives, a recruté...


Avec un secteur du CBD européen en pleine expansion, malgré un bourbier réglementaire, des centaines d’acteurs industriels de part et d’autre de l’Atlantique sont confrontés à...
Des chercheurs américains ont analysé 28 récentes études, pour observer l’état des connaissances scientifiques sur l’utilité du cannabis contre la sclérose en plaques. Ce procédé –...


Jazz Pharmaceuticals, société pharmaceutique irlandaise, a annoncé avoir conclu un accord pour acheter 7,2 milliards $ (6 milliards €) en espèces et en actions le fabricant...


La prescription et le remboursement de deux médicaments à base de cannabis ont été approuvés par le système de santé publique anglais (NHS). L’organisme de surveillance...


Au Royaume-Uni, le cannabis médical a été légalisé l’année dernière, après que les parents d’Alfie Dingley et de Billy Caldwell, tous deux atteints d’épilepsie résistante aux traitements,...


Certaines études préliminaires suggèrent que le cannabis pourrait être efficace dans le traitement d’Alzheimer. La maladie d’Alzheimer s’accompagne bien souvent d’une forme de démence, une pathologie...


Alors que les recherches sur les possibilités du cannabis et ses vertus thérapeutiques commencent à se multiplier, tous les pays ne mettent pas à disposition les...
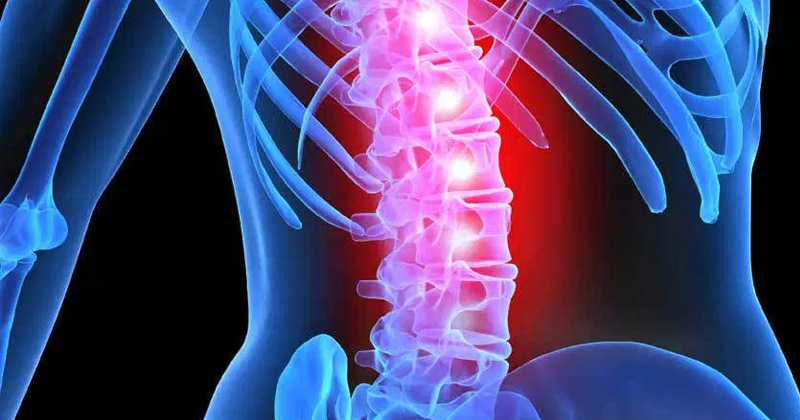

De nouvelles recherches indiquent que le Sativex, un spray à base de phytocannabinoïdes peut atténuer la spasticité associée à une lésion prolongée de la moelle épinière....

GW Pharmaceuticals annonce des résultats positifs de phase II de leur test clinique sur le glioblastome récidivant, une des tumeurs au cerveau les plus courantes et particulièrement...
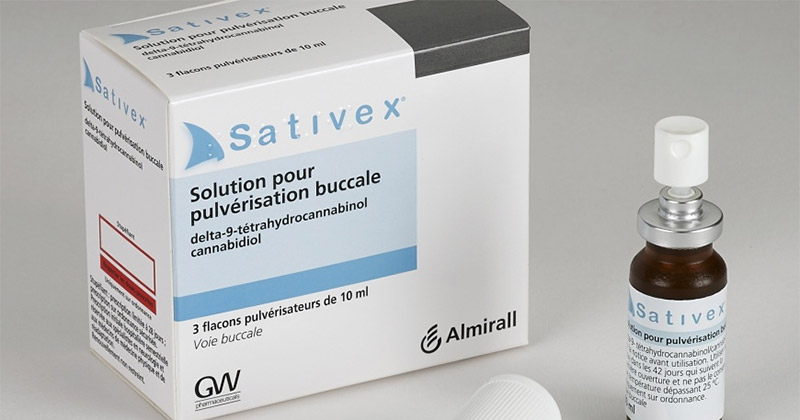

Nous parlons souvent ici du Sativex, le seul médicament à base de cannabis naturel autorisé à la vente en France. Ce spray oral contenant CBD et...
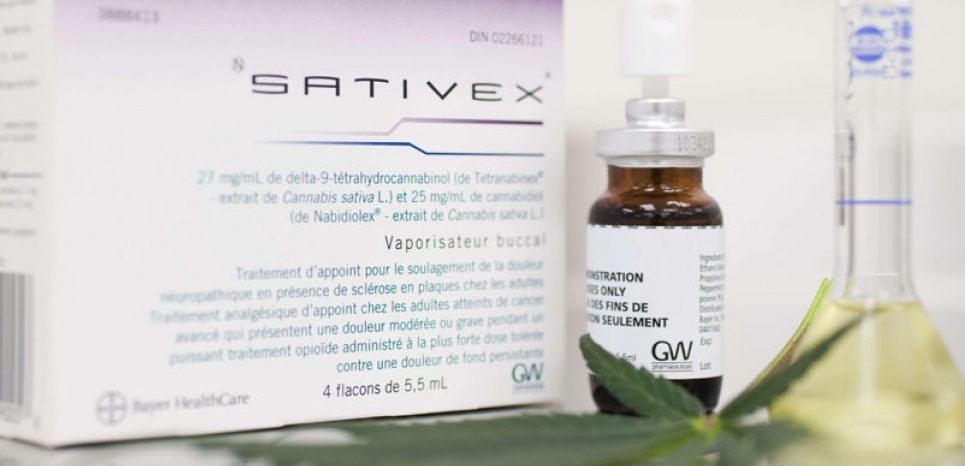

L’agence Nationale de la Santé Brésilienne (ANVISA) a annoncé le 16 janvier la mise en rayons pharmaceutiques du Mevatyl de l’Anglais GW Pharmaceutical. Ce médicament tiré...


L’Union Francophone pour les Cannabinoïdes en Médecine organise le 21 octobre à Strasbourg la 5ème (et seule) conférence française internationale sur le cannabis thérapeutique. L’événement gratuit et ouvert...
Vous devez être connecté pour poster un commentaire.